Dans les premiers temps de la chimie organique, chaque nouveau composé recevait un nom trivial, généralement relié à la provenance du composé. Toutefois, il devint vite évident, vu le très grand nombre de composés organiques possibles à cause de l'isomérie, qu'une méthode systématique était nécessaire pour attribuer automatiquement et sans ambiguïté un nom à tout nouveau composé organique aussitôt qu'il était synthétisé ou découvert. Un système international de nomenclature a donc été conçu et il est reconnu et utilisé par tous les chimistes organiciens du monde. Ce système a été recommandé par l'Union international de Chimie pure et appliquée, habituellement désignée par le sigle "UICPA".
Régles de l'UICPA pour les hydrocarbures saturés acycliques
1. Le nom
générique des membres de la série est alcanes; tous les noms
portent la terminaison -ane. Les composés non ramifiés sont
nommés conformément au tableau ci-dessous et ces noms
constituent également la base pour les noms des composés
comportant des structures ramifiées. Il faut donc les apprendre.
| Nombre de carbones | Formule | Nom |
| 1 | CH4 | Méthane |
| 2 | CH3CH3 | Éthane |
| 3 | CH3CH2CH3 | Propane |
| 4 | CH3CH2CH2CH3 | Butane |
| 5 | CH3CH2CH2CH2CH3 | Pentane |
| 6 | CH3CH2CH2CH2CH2CH3 | Hexane |
| 7 | CH3CH2CH2CH2CH2CH2CH3 | Heptane |
| 8 | CH3CH2CH2CH2CH2CH2CH2CH3 | Octane |
| 9 | CH3CH2CH2CH2CH2CH2CH2CH2CH3 | Nonane |
| 10 | CH3CH2CH2CH2CH2CH2CH2CH2CH2CH3 | Décane |
2. Pour nommer un composé à structure ramifiée, il faut identifier la chaîne carbonée linéaire la plus longue présente dans la molécule. Cette chaîne est nommée d'après le nombre d'atomes de carbone qu'elle contient (tableau ci-dessus).
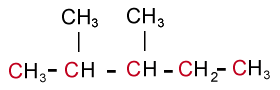
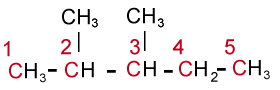
Par exemple, dans la structure ci-dessous, la chaîne linéaire la plus longue (les C de couleur) comporte cinq atomes de carbones; le nom du composé est donc attribué comme s'il s'agissait d'un dérivé du pentane (même si le composé compte au total sept atomes de carbone et est un isomère de l'heptane, C7H16).

3. On numérote la chaîne carbonée à partie de l’extrémité, de façon telle que les carbones qui portent les ramifications ou les regroupements aient les plus petits numéros possible. Dans notre exemple, la chaîne est numérotée à partie de la gauche, de façon à ce que les regroupements soient sur les carbones 2 et 3 (et non 3 et 4, obtenus en partant la numérotation de la droite).
4. Les regroupements portés par la chaîne principale sont appelés substituants. Les substituants saturés qui ne contiennent que du carbone et de l’hydrogène sont appelés groupes alkyles. Ils sont nommés d’après l’alcane ayant le même nombre d’atomes de carbone en remplacent la terminaison -ane par celui de -yle.
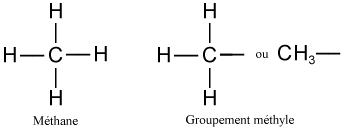
Dans l’exemple ci dessus, chaque substituant ne compte qu’un atome de carbone. Un tel substituant dérive du méthane par la perte d’un hydrogène st s’appelle groupement méthyle.
Le groupe alkyle à deux carbones est appelé éthyle, d'après l'éthane.

Deux groupements peuvent être obtenus à partir du propane, selon l'hydrogène qui est enlevé.
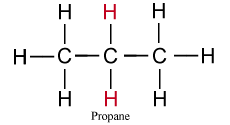
Si on enlève un hydrogène terminal (en noir), on obtient le groupement normal ou n-propyle.
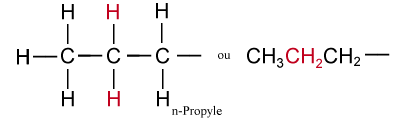
Tandis que si l'on enlève un hydrogène central (en couleur), on obtient le groupement isopropyle.
![]()